Neue Wirkstoffe gegen widerständige Keime

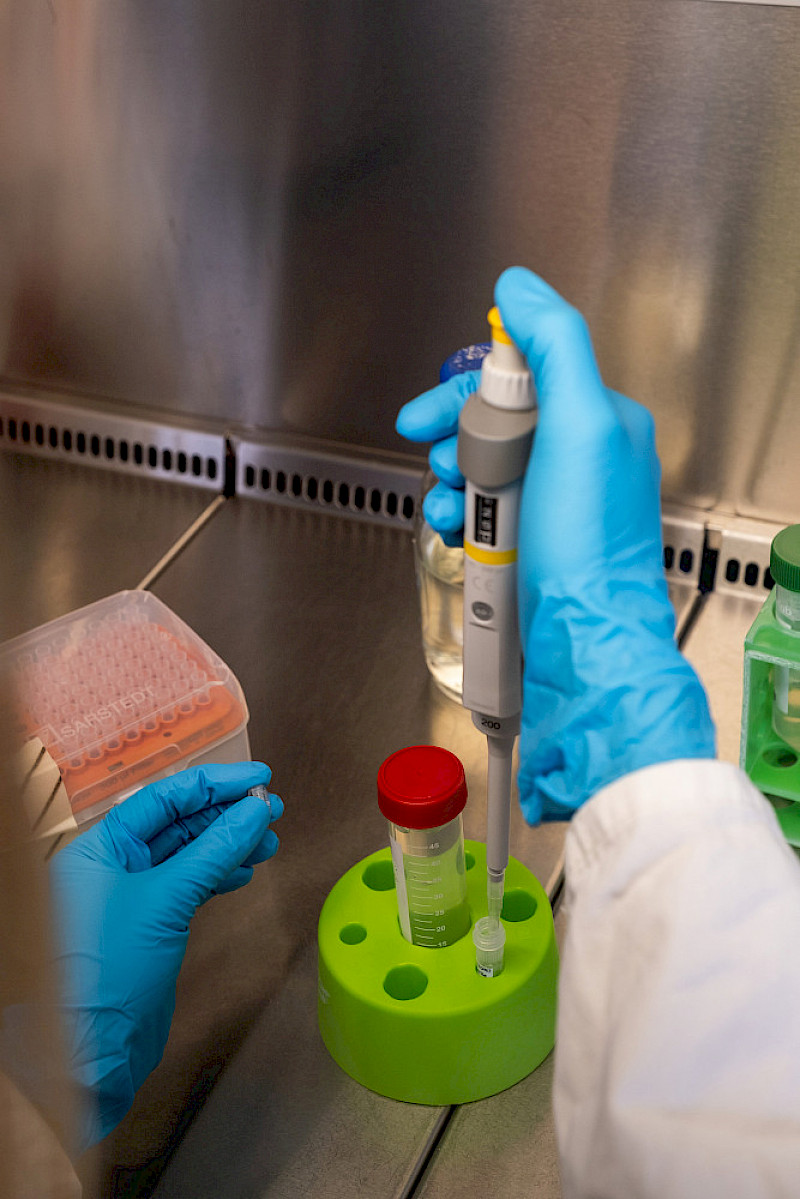
Wenn Lea Mann morgens das Institut für Pharmazie auf dem Weinberg in Halle betritt, zieht es sie meist direkt ins Labor. Dort streift sie ihren weißen Kittel und Einweghandschuhe über, legt ihre Schutzbrille an und widmet sich mikrobiologischen Experimenten. Grundlagenforschung also. Sie arbeitet als Doktorandin in einem von der Deutschen Forschungsgemeinschaft finanzierten Projekt, bei dem es um die Synthese, Charakterisierung, Testung und Optimierung neuer Wirkstoffe gegen das antibiotikaresistente Bakterium M. abscessus geht. Geleitet wird es von Dr. Adrian Richter, der sich am Institut für Pharmazie über neue Therapiemöglichkeiten dieses Keims habilitiert.
Diese Forschung ist dringlich. Denn multiresistente Bakterienstämme treten immer häufiger auf. Und M. abscessus ist besonders hartnäckig. Er nistet sich in der Lunge ein und kann das dortige Gewebe stark schädigen. Besonders gefährdet sind Menschen mit chronischen Lungenerkrankungen. In den letzten Jahren haben sich weltweit beispielsweise immer mehr Personen infiziert, die bereits mit der angeborenen Stoffwechselstörung Mukoviszidose vorerkrankt sind.
„Bislang ist die Behandlung solcher bakteriellen Infektionen schwierig und langwierig“, sagt Richter. Denn zum einen ist der Keim von Natur aus resistent gegen viele Antibiotika, zum anderen reicht die Konzentration, mit der die bisherigen Wirkstoffe in das infizierte Gewebe gelangen, häufig nicht aus.
Chemische Abwandlungen als Wirkstoff-Kandidaten
Das Projekt startete im Juni 2019 an der MLU – mittlerweile sind die ersten Meilensteine erreicht. Während eines Forschungsaufenthalts an der University of British Columbia in Kanada hatte Richter bereits im Vorfeld umfangreiche Tests mit 500 Substanzen durchgeführt. Ziel war es, Verbindungen zu finden, die das Wachstum des Bakteriums deutlich hemmen. Anschließend wurden die Strukturen dreier ausgewählter Verbindungen chemisch verändert, um deren Eigenschaften weiter zu verbessern. „Anhand eines Syntheseplans haben wir daraus mittlerweile rund 65 chemische Analoga der ursprünglichen Substanzen hergestellt, gereinigt und charakterisiert“, erklärt Doktorandin Mann, die insbesondere für die mikrobiologische Charakterisierung zuständig ist. Diese neuen Wirkstoff-Kandidaten werden nun in einem speziellen Sicherheits-Labor des Kooperationspartners Fraunhofer-Institut für Zelltherapie und Immunologie (IZI) weiter erprobt und optimiert.
In ihrem Arbeitsalltag profitieren die Forschenden davon, in der Abteilung Pharmazeutische Chemie unter Leitung von Prof. Dr. Peter Imming eine umfangreiche experimentelle Ausstattung und eine gut funktionierende multidisziplinäre Zusammenarbeit vorzufinden. So können sie eng verzahnt die chemischen und mikrobiologischen Methoden anwenden, die Verbindungen weiterentwickeln und direkt testen. „Die kurzen Wege beschleunigen das Projekt und ermöglichen ganz neue experimentelle Zugänge. Wir müssen die Substanz nicht immer zu einem weit entfernten Kooperationspartner schicken und dann erst mal abwarten. Wir können vor Ort von der Syntheselaborbank bei uns direkt ins Mikrobiologie-Labor des IZI gehen und die Tests selbst durchführen. So gewinnen wir ein viel besseres Verständnis“, sagt Richter.
„Und wir können die Wachstumsbedingungen der Erreger gezielt beeinflussen“, ergänzt Mann. „Beispielsweise indem wir sie Nährstoffmangel aussetzen oder verschiedene Wachstumsmedien nutzen.“
Wachstum der Bakterien mit Fluoreszenzmikroskopie beobachten
Die neuen Substanzen werden auch spezifisch im Kontext von Mukoviszidose untersucht: Mit 152.000 Euro fördert der Mukoviszidose e. V. ein Teilprojekt, das sich mit einer speziellen und komplexen Testmethode befasst. Im Fokus stehen dabei Interaktionen und Synergien mit etablierten antibakteriellen Medikamenten und mit typischen Mukoviszidose-Medikamenten. Derzeit kultiviert das Team die Mykobakterien im Labor und analysiert in Kooperation mit dem Fraunhofer IZI die Aktivität der neuen Verbindungen dort in vitro, also in der Petrischale. „So finden wir heraus, ob unsere neuen Substanzen das bakterielle Wachstum tatsächlich hemmen und die Erreger ausschalten können. Das gewünschte Ergebnis heißt bakterizid. Denn das ist eine wichtige Eigenschaft eines Antibiotikums“, erklärt Richter.
Da die Erreger auch Makrophagen, also menschliche Immunzellen, infizieren und deren Abwehrmechanismen hemmen können, simulieren die Wissenschaftlerinnen und Wissenschaftler diese Vorgänge mit einem eigens entwickelten Screening-Verfahren im Labor: Sie infizieren die Immunzellen mit den Bakterien und züchten sie in Gegenwart eines Wirkstoffs an. Drei Tage später lässt sich die Hemmwirkung dann mit Fluoreszenzmikroskopie untersuchen.
Wirksamer um den Faktor 15, aber noch instabil
Eine wichtige Eigenschaft für das spätere Medikament liegt darin, dass die Hemmstoffe auch in sehr hohen Verdünnungen wirken müssen. Den Forschenden ist es bislang gelungen, Verbindungen zu erzeugen, die um den Faktor 10 oder 15 wirksamer sind als die Ausgangsverbindung. „Sie unterdrücken das Bakterienwachstum also sehr viel effizienter. Und sie sind schon in geringer Konzentration in der Lage, die Bakterien so stark zu schädigen, dass sie nicht mehr nachwachsen können“, sagt Richter.
Eine Hürde gilt es allerdings noch aus dem Weg zu räumen: Die neuen Verbindungen werden derzeit noch zu schnell abgebaut, sobald sie in einen Organismus übertragen werden. Das nächste Ziel ist es daher, die Hintergründe aufzuklären: Was geschieht da? Und wie lässt sich die Struktur so optimieren, dass sie stabil genug ist?
Sobald diese Fragen geklärt sind, wäre ein weiterer Meilenstein des Projekts erreicht: einen Wirkstoff mit vielversprechenden präklinischen Eigenschaften zu entwickeln. „Nach gelungener Optimierung, wenn der Wirkstoff also bioverfügbar ist, könnten wir gemeinsam mit Kooperationspartnern zu einer In-vivo-Tierstudie übergehen“, sagt Richter. „Vielversprechend wäre das Ergebnis für uns, wenn unsere Substanz in einem lebenden Organismus die Anzahl der Bakterien besser mindern kann als die derzeit eingesetzten Wirkstoffe.“
Um diese irgendwann zu marktreifen Medikamenten weiterzuentwickeln, wären in einem anderen Rahmen groß angelegte klinische Studien nötig, in denen die Wirksamkeit am Menschen erprobt wird. Richter betont jedoch: „Die Entwicklung neuer antibiotischer Wirkstoffe ist immens wichtig, besonders wegen ihres schnellen und großen therapeutischen Benefits.“
Mukoviszidose
In Deutschland sind mehr als 8.000 Kinder, Jugendliche und Erwachsene von Mukoviszidose betroffen. Durch eine Störung des Salz- und Wasserhaushalts im Körper bildet sich bei Mukoviszidose-Betroffenen ein zähflüssiges Sekret, das Organe wie die Lunge und die Bauchspeicheldrüse irreparabel schädigt. Jedes Jahr werden allein in Deutschland etwa 150 bis 200 Kinder mit der seltenen Krankheit geboren.